

En el manejo de estanques, es necesaria una suficiente cantidad de agua para compensar las pérdidas por evaporación y filtración, así como para remover metabolitos producidos por la actividad biológica de los peces y otros organismos acuáticos; debe complementarse con agua de buena calidad que proporcione el ambiente apropiado para que los peces se desarrollen en condiciones favorables, que permitan obtener las mejores producciones por área.
La calidad de agua viene dada por ciertas propiedades físicas y químicas, que responden al tiempo y clima locales, a la naturaleza del suelo, así como a la actividad biológica de los organismos que la habitan.
El piscicultor debe tener un buen entendimiento del tiempo y clima locales. Como las variables cambian con la estación y como dichos cambios pueden ser esperados año a año, debe conocer los valores normales y extremos de las variables meteorológicas, como la temperatura del aire, radiación solar, cubierta de nubes, vientos y precipitación, entre otros.
La radiación solar, indispensable para la función fotosintética, afecta directamente a la temperatura, así los lugares más calientes son aquellos con mayor radiación solar, que a su vez es afectada por la transparencia de la atmósfera a causa del polvo atmosférico, vapor de agua y distancia que la luz tiene que viajar desde la fuente hasta la superficie terrestre.
La temperatura está relacionada inversamente a la latitud. Las latitudes más altas son más frías, en tanto que en el Ecuador la temperatura es más elevada, de no mediar factores moderadores como la elevación y los cuerpos de agua. Por ejemplo Quito, que está a una latitud de 0 , pero tiene una temperatura de un clima templado a causa de su altitud sobre el nivel del mar (2 800 msnm).
La influencia del viento es importante en la piscicultura, pues hace circular el agua del estanque, favoreciendo su oxigenación; asimismo la evaporación se ve favorecida con el aumento de la velocidad del viento.
La influencia de la lluvia está fuera de toda discusión, pues es la causa que determina el retorno del agua de la atmósfera a la superficie terrestre, haciéndola disponible para múltiples usos. En el caso de la Amazonía la piscicultura se ve favorecida con un nivel apropiado de precipitación. Sin embargo, los valores elevados son inconvenientes pues remueven rápidamente los nutrientes del agua, necesarios para la producción biológica, fundamentalmente en los estanques de presa.
Se entiende entonces, la necesidad que tiene el piscicultor de conocer las condiciones meteorológicas de la zona, porque por un lado están más disponibles los datos meteorológicos que los hidrobiológicos, si es que existen; y con los primeros se puede inferir variaciones del agua así como sus bondades para estanques, mejor aún si se relaciona con la naturaleza del suelo, magnitud del valle, etc.
La influencia de la temperatura se da no solamente en forma directa sobre los peces, sino también rige a otros parámetros, tales como la evaporación, la solubilidad de los gases, la actividad de los organismos desintegradores del fondo, que transformen la materia orgánica en sustancias inorgánicas nutritivas.
Se entiende claramente la influencia decisiva de la temperatura en los peces por tratarse de organismos que no tienen capacidad de autoregular la temperatura corporal, la que depende de su medio ambiente, (organismos poiquilotermos o de sangre fría). En tanto que los homotermos son los que regulan su temperatura corporal y la conservan en un valor, aún cuando la temperatura ambiental fluctúa grandemente, como es el caso de los mamíferos.
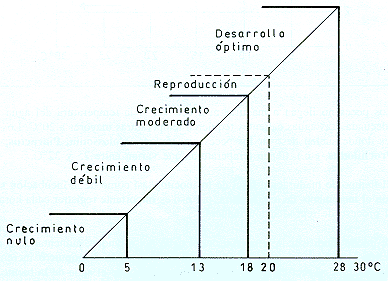
Cada especie tiene límites de tolerancia más o menos amplios aunque su desarrollo óptimo se da dentro de un rango más estrecho, como sucede con el crecimiento; el aumento de la tasa metabólica con la temperatura; en tanto que a valores bajos los peces de aguas cálidas, como los amazónicos, disminuyen su tasa de crecimiento, llegando incluso a paralizarse. (Fig. 3.1).
Fig. 3.1: Influencia de la temperatura en el crecimiento de los pece
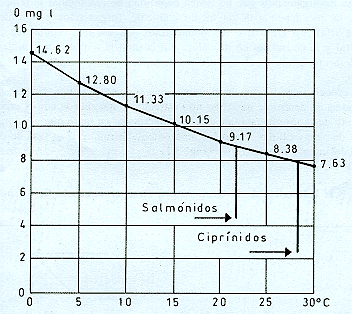
En la respiración de los peces la temperatura influencia indirectamente, al condicionar la concentración de oxígeno disuelto en el agua, pues están relacionados inversamente. Así se observa en agua pura, que a 0 C la concentración de oxígeno disuelto es de 14,62 mg/l, 9,17 mg/l a 20 C, y 7,63 mg/l a 30 C. (Fig. 3.2).
Fig. 3.2: Influencia de la temperatura en la concentración de oxígeno disuelto en el agua.
Los peces no llegan a madurar ni a desovar si la temperatura del agua no es la adecuada. Las aguas calientes requieren temperaturas mayores a 20 C. Los ambientes donde suelen desovar los peces amazónicos (Colossoma, Piaractus, Brycon, Prochilodus, etc.), tienen temperaturas que varían entre 25 y 32 C.
El tiempo de maduración final de los oocitos, así como de la incubación se reduce con el incremento de temperatura, por eso es importante registrar cada hora durante el proceso de reproducción inducida.
Se puede modificar la temperatura del agua del estanque, aumentando o disminuyendo el caudal del agua de alimentación, que puede disminuir o incrementar la temperatura respectivamente; esto es obvio desde que el agua de la fuente siempre será más fría que la del estanque, que por su gran superficie, recibe mayor radiación solar, calentándola.
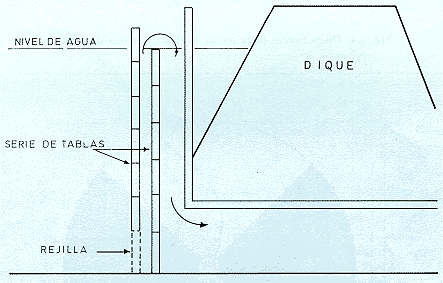
Debido a la estratificación termal de la columna de agua de un estanque, en que aguas más calientes están en la superficie, por la insolación y aguas más frías en el fondo; es posible elevar la temperatura del agua de un estanque eliminando el agua del fondo, mediante un monje de tipo Herrguth (Fig. 3.3) que saca agua fría del fondo y lo compensa por agua de la fuente que ingresa por la superficie, que comparativamente tiene mayor temperatura.
Fig. 3.3: Monje de desague tipo Herrguth para evacuación del agua del fondo del estanque
La transparencia o claridad del agua permite mayor o menor penetración de la luz, factor indispensable para el desarrollo de los organismos verdes (algas), inicio de la producción biológica en el estanque.
La turbidez del agua se debe al material en suspensión, mineral u orgánico. Limita la penetración de la luz disminuyendo la transparencia, y, por ende, la producción primaria. Sin embargo, la turbidez causada por el plancton es una condición deseada, al contrario de la producida por partículas en suspensión, como las de arcilla u otras sustancias húmicas coloidales que pueden adosarse a las branquias, reduciendo la superficie respiratoria de las laminillas branquiales. Por otro lado la turbidez afecta la habilidad de los peces para aprehender el alimento, perdiéndose en el fondo e incrementando a la vez el material orgánico, cuya descomposición exige mayor cantidad de oxígeno disuelto.
Una anotación útil en piscicultura es el "punto de compensación", profundidad a la cual se encuentra el 1% de la luz incidente en la superficie del agua. Este punto limita la zona eufótica o zona productiva, en la cual la tasa de fotosíntesis excede a la tasa respiratoria, y que varía entre 0,5 a 1,0 m de profundidad.
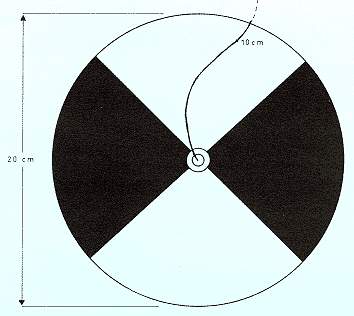
La transparencia se mide mediante el "disco Secchi" (Fig. 3.4), consistente en un disco metálico de aproximadamente 30 cm de diámetro, pintado de negro y blanco alternado en cuatro secciones, que lleva una cuerda calibrada sujeta al centro de una cara, que permite medir a qué profundidad desaparece de la vista, siendo este dato el registrado como medida de la transparencia.
Fig. 3.4: Disco Secchi para medir la transparencia del agu
La turbidez alta a causa de material en suspensión, puede disminuir añadiendo sulfato de aluminio (AlSO4) o "alumbre", que precipita el material clarificando el agua. Algunas plantas acuáticas (Salvinia, Pistia y Eichornia) clarifican también el agua.
El color del agua está determinado por las impurezas en ella contenidas y la incidencia de los rayos solares. Se modifica a causa de varios factores, como los florecimientos filoplanctónicos que le comunican una coloración verdosa, dependiendo también de la especie predominante como las Cianofitas, que tienen tono azulado; las sustancias húmicas, originadas en material vegetal en descomposición, comunican al agua un color oscuro o "agua negra".
La conductividad es una de las mejores medidas de la riqueza del agua y está dada por los iones disueltos en ella. Se expresa en microhom/cm y se mide mediante el "conductivímetro".
Está directamente relacionada a la salinidad, que para agua dulce le corresponde a la concentración de todos los iones disueltos, los mismos que determinan la presión osmótica del agua a la que deben adaptarse las diferentes especies de peces.
Gran parte de los sólidos disueltos se originan por el contacto del agua con las rocas y el suelo; se menciona que la composición de minerales disueltos en el agua se debe al clima, geología local, topografía, biología del agua y al estado del tiempo. Los iones más frecuentes son: calcio, magnesio, sodio, potasio, carbonatos, sulfatos y cloruros.
El contenido del oxígeno disuelto en el agua de los estanques es sin duda alguna el más crítico entre los factores de calidad del agua; si no se mantiene en niveles apropiados en forma constante, los peces se afectan, no comen mientras las condiciones de baja concentración de oxígeno persisten y aún recuperando el nivel apropiado este comportamiento se prolonga por algún tiempo más, haciendo a los peces susceptibles a las enfermedades. Por otro lado este hecho eleva la tasa de conversión alimentaria y consecuentemente los costos de producción, o sea, se requiere mayor cantidad de alimentos para producir igual carne de pescado.
Si bien algunas especies, como las exóticas "tilapias" y las nativas "gamitana" y "paco" pueden tolerar niveles bajos de oxígeno disuelto, está demostrado como las funciones vitales se ven afectadas cuando se registran tenores bajos de oxígeno disuelto, en un período prolongado, dando como resultado la disminución o paralización de la tasa de crecimiento, lo que obviamente perjudica al piscicultor.
Cuando el nivel de oxígeno disuelto cae por debajo del rango normal, los peces suben a la superficie del agua, buscando tomar directamente el oxígeno atmosférico, para lo cual se adaptan con el rápido desarrollo del labio inferior que le facilita tomar más fácilmente el oxígeno. Este comportamiento es fácil comprobar entre 5-7 am, pues todos o casi todos los peces lo realizan al mismo tiempo, acción que recibe la denominación de "boquear".
El oxígeno disuelto del agua de los estanques proviene principalmente del oxígeno atmosférico, en el que se encuentra mezclado con otros gases como nitrógeno, argón, y dióxido de carbono, entre otros. Cuando el aire entra en contacto con el agua, el oxígeno se difunde en ella hasta que la presión de este elemento en el agua se iguale a la presión que tiene en el aire. Pero, más que tratar de la presión del oxígeno disuelto, es conveniente expresar la solubilidad en mg de oxígeno por litro de agua. Esta solubilidad decrece con el aumento de la temperatura e incremento de la salinidad; aunque para este último caso tratándose de estanques de agua dulce su influencia puede ignorarse.
En el agua la concentración de oxígeno disuelto está cambiando constantemente por causa de procesos biológicos, físicos y químicos. Por su parte el aire sobre el estanque puede considerarse que tiene un porcentaje constante de oxígeno, pudiendo variar levemente de acuerdo a la presión atmosférica del lugar.
Cuando la presión del oxígeno en el agua está en equilibrio con el oxígeno atmosférico no hay transferencia de este elemento entre el aire y el agua. La transferencia ocurre cuando el agua está insaturada con oxígeno disuelto. Sin embargo, cuando el agua está sobresaturada de oxígeno, también ocurre la transferencia hacia el aire.
Para aguas tranquilas la transferencia de oxígeno dependerá de:
Como los cuerpos de agua naturales (también los estanques) no están nunca completamente quietos, la transferencia de oxígeno es regulada por la cantidad de turbulencia que incrementa el área de la interfase aire-agua.
Los procesos biológicos son tanto o más importantes que los procesos físicos descritos en la regulación de la concentración de oxígeno disuelto en el agua de un estanque. Las plantas, incluido el fitoplancton, que crecen en los estanques producen oxígeno mediante la fotosíntesis, como se observa en la ecuación global.
6CO2 + 6H2O C6H12O6 + 6O2
Se espera por tal razón, que la cantidad de oxígeno producido por la fotosíntesis en las aguas superficiales de un estanque sea una función de la abundancia del fitoplancton.
Este proceso es controlado por factores como: temperatura, luz, concentración de nutrientes, especies y abundancia de plantas, y turbulencia, entre otros.
Por otro lado, los organismos consumen el oxígeno en su respiración, que desde un punto de vista práctico puede considerarse como un proceso inverso a la fotosíntesis, como se observa sumariamente en la ecuación.
C6H12O6 + 6O2 6CO2 + 6H2O + calo
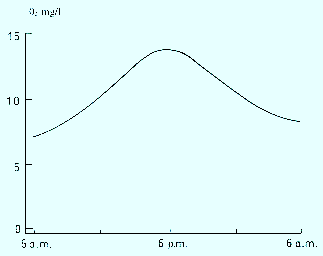
Obviamente en estanques donde la fotosíntesis está progresando más rápidamente que la respiración el consumo de CO2 es alto al igual que la liberación de oxígeno cuya concentración es alta. Esto es usual en horas y lugares donde la intensidad de la luz es alta y los organismos verdes son abundantes. Cuando la respiración excede a la fotosíntesis la situación es contraria, lo que se observa durante la noche registrándose las menores concentraciones de oxígeno disuelto en la madrugada. (Fig. 3.5)
Fig. 3.5: Variación del oxígeno disuelto durante el dí
3.2.5.1 REQUERIMIENTO DE OXIGENO DISUELTO
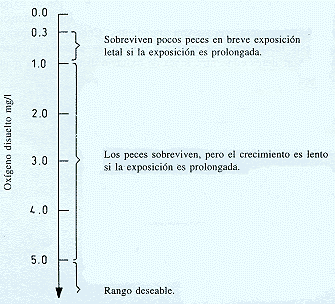
Para peces de agua caliente, con propósitos prácticos se considera que una concentración de oxígeno disuelto menor que 5,0 mg/l es indeseable (Fig. 3.6). Aunque se soporta la supervivencia a menores concentraciones, siempre que el nivel de dióxido de carbono libre sea también bajo; sin embargo de todos modos la exposición prolongada a bajos niveles de oxígeno disuelto siempre es dañino para el pez.
Fig. 3.6: Efecto de la concentración de oxígeno disuelto sobre peces de agua caliente en cultivo.
Al igual que en los otros vertebrados, la sangre de los peces contiene la hemoglobina - Hb - que interviene en el transporte del oxígeno en la sangre, la misma que es regulada por la tensión de este gas; así, en las laminillas branquiales la tensión del oxígeno es más álta y se carga a la Hb de la sangre. En los tejidos el oxígeno es usado rápidamente, así la Hb descarga el oxígeno en los fluidos del tejido. La reacción que se da a nivel de branquias puede ilustrarse con la fórmula:
Hb + O2 HbO2. Lo contrario sucede a nivel de tejidos.
La relación entre la tensión del oxígeno y el porcentaje de saturación de hemoglobina con O2 se conoce como la "curva de disociación de oxihemoglobina", que toma las formas hiperbólica y sigmoidea según se traten de especies de aguas frías y calientes, respectivamente.
La cantidad de oxígeno requerido por los animales acuáticos varía grandemente y depende de las especies, tamaño, alimento, actividad, temperatura del agua y concentración de oxígeno disuelto. Por ejemplo un pez que recién comió consume oxígeno más rápidamente que un pez en ayuno y la tasa de consumo de oxígeno crece con el incremento de actividad y la respiración se incrementa con la temperatura. Se reporta que por cada 10 C de incremento de la temperatura del agua, el consumo de oxígeno se dobla. La composición del cuerpo afecta al consumo de oxígeno, así se observó que en el "bagre del canal" los peces más flacos consumen menos oxígeno que los gordos, etc.
La sobresaturación con gases, entre ellos el oxígeno, también es dañina y en muchos casos causa el "TRAUMA DE LA BURBUJA DE GAS", que consiste en la formación de burbujas gaseosas en la sangre y tejidos, causando problemas agudos y crónicos. Los huevos flotan en la superficie; larvas, post larvas y los más pequeños muestran hiperinflación de la vejiga gaseosa, edema, e hinchazón de laminillas branquiales. En juveniles y adultos lo más común es la burbuja de gas en sangre y tejidos, conjuntamente con la proyección de los ojos.
La sobresaturación suele darse cuando se presenta una floración fitoplanctónica en la superficie, en este caso los peces suelen nadar en las aguas más profundas donde la sobresaturación es menor.
3.2.5.2 MEJORAMIENTO DE LA CONCENTRACION DE OXIGENO DISUELTO
Como se anotó anteriormente, el oxígeno disuelto es la variable más crítica de la calidad del agua en piscicultura semiintensiva e intensiva, por lo que es necesario tener los mecanismos para superar la depleción del oxígeno, que puede matar o afectar severamente a los animales acuáticos.
El método más utilizado consiste en dar mayor flujo al ingreso de agua que por ser corriente debe tener mayor concentración de oxígeno y por otro lado en el recorrido del canal se puede crear cascadas o turbulencias para incrementar la superficie de la interfase aire-agua. De igual forma el tubo de ingreso de agua al estanque puede tener múltiples perforaciones para dispersar el agua para una mejor aireación e igualmente el agua que ingresa puede caer sobre una especie de tamiz, que cumple la misma función.
La eliminación de agua del fondo, casi siempre con menor tenor de oxígeno y más fría, puede hacerse con un monje tipo HERRGUTH, ya citado (Fig. 3.3). La eliminación del agua más fría del fondo del estanque es reemplazada rápidamente con el mayor caudal del canal de alimentación.
Otros sistemas que incluyen equipos mecánicos, como ruedas de paletas difusoras de aire (3.7), no se tiene referencias de su uso en la región, pero debe considerarse para disminuir riesgos en casos críticos. Pueden funcionar con motores eléctricos o con motores autónomos (Figs. 3.7b). También se puede oxigenar el agua del estanque pasando una manguera o ducto plástico perforado que recorre el fondo del estanque y por el que se inyecta oxígeno (Fig. 3.8).
Dependiendo de la escala en que se practica la piscicultura, el monitoraje del oxígeno disuelto es necesario realizarlo diariamente, sobre todo al amanecer que es cuando se presentan los niveles más bajos.
Fig. 3.7: Rueda de paletas difusora de aire en los estanques de piscicultur
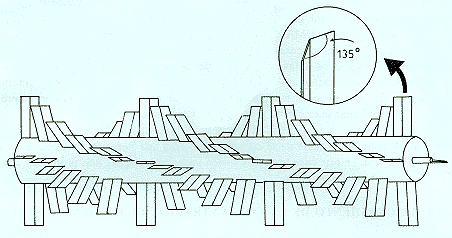
Fig. 3.7b: Rueda de paletas para oxigenar el agua de un estanqu
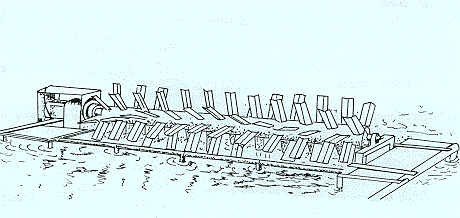
Fig. 3.8: Tubo con perforaciones para airear el agua del estanqu

El clásico método volumétrico de Winkler y del oxímetro proveen de información de exactitud al 0,1 mg/l. Mientras que el primero toma unos minutos, requiere reactivos químicos, material de vidrio incluyendo la bureta de titración; el oxímetro es enteramente confiable, exige el reemplazo de la membrana que cubre el final de la sonda, así como el cambio de líquido dentro de la sonda.
Un oxímetro de buena calidad puede costar algunos cientos de dólares (algunos miles en la región), en tanto que los kits de titración son más baratos, pero requieren reemplazo periódico. Resumiendo, con el oxímetro se ahorra tiempo y la necesidad de reponer químicos y equipo roto, lo que hace del oxímetro la selección más económica a largo plazo.
El dióxido de carbono es un constituyente menor de la atmósfera (0,032%) y es altamente soluble en agua, comportándose como un ácido, tal como se observa en la ecuación que sigue:
H+
CO2 + H2O=H2CO3
HCO3
El agua pura, saturada con CO2 a 25 C y a presión atmosférica estándar tiene una concentración total de 0,46 mg/l y teóricamente tendrá un pH de 5,68. A más grandes concentraciones de dióxido de carbono el pH será menor, así, si la concentración es 30 mg/l a 25 C, el pH será aproximadamente 4,8.
El dióxido de carbono del agua usualmente es una función de la actividad biológica. La respiración es un proceso mucho más rápido que la fotosíntesis y el dióxido de carbono se acumula. Por la madrugada el agua está saturada de dióxido de carbono.
Concentraciones altas de dióxido de carbono tienen efectos narcóticos sobre los peces y pueden llegar a causar la muerte, porque el ingreso del CO2 al organismo del pez se hace por difusión a través de las branquias.
La alta concentración de este gas en el agua baja la tasa de eliminación al medio, acumulándose en la sangre, con la consiguiente disminución del pH, lo que causa efectos nocivos. También la alta concentración de CO2 interfiere con la oxigenación de la hemoglobina.
Los peces pueden sentir pequeñas diferencias en la concentración de dióxido de carbono libre e intentarán escapar de áreas con altas concentraciones, aunque 10 mg/l pueden ser toleradas si hay una alta concentración de oxígeno disuelto.
En estanques de piscicultura intensiva el dióxido de carbono libre fluctúa de 0 mg/l en la tarde a 5-10 mg/l al amanecer, con claros efectos sobre el pez.
3.2.7 ALCALINIDAD TOTAL Y DUREZA TOTAL
La alcalinidad es una medida de la concentración de iones carbonato y bicarbonato en el agua y se expresa en mg/l de carbono de calcio equivalente. La presencia de los iones le confieren al agua una capacidad amortiguadora del pH, y, en consecuencia a mayor concentración de carbonato y bicarbonato el pH del agua se mantendrá más estable en valores altos. Al contrario la baja alcalinidad facilita los cambios del pH en un perfil de 24 horas.
En piscicultura la alcalinidad estaría generalmente entre 30 y 200 mg/l de CaCO3 equivalente; aunque alcalinidades más altas o más bajas no perjudicarán en los cultivos.
Se puede aumentar la alcalinidad y la dureza pasando el agua a través de camas de piedras caliza chancada o conchas de ostras.
Por su parte la dureza total está determinada por la concentración de cationes divalentes, principalmente calcio y magnesio, y se expresa en mg/l de CO3Ca equivalente. Según la dureza el agua se clasifica en:
En piscicultura las mejores aguas, respecto a la alcalinidad y dureza, se dan cuando tienen valores similares. Cuando existe mucha diferencia el pH puede variar fuertemente, fundamentalmente subir a niveles altos durante la fotosíntesis.
Se puede corregir estos parámetros, cuando son muy bajos, mediante el encalamiento, pero es imposible bajarlos cuando tienen niveles elevados.
Es el logaritmo negativo de la concentración de hidrogeniones. En términos prácticos, mide el grado de acidez y alcalinidad del agua. Se mide en una escala de 1 a 14. La mayoría de aguas naturales tienen un pH que varía entre 5 y 10.
Como ya se vio anteriormente, el dióxido de carbono al asociarse con el agua: CO2 + H2O=H2CO3 forma ácido carbónico que rápidamente se disocia en iones H+ y HCO3-. Se espera en consecuencia, que a mayor concentración de dióxido de carbono el pH será menor.
Durante el día los vegetales acuáticos usan el dióxido de carbono del agua para la fotosíntesis, las plantas y animales liberan en el agua dióxido de carbono producido por la respiración, que es usado rápidamente por las plantas acuáticas, incrementándose el pH. Pero la figura se invierte en la noche en que la fotosíntesis es nula en tanto que la respiración continúa produciendo dióxido de carbono, lo que hace bajar el pH a su mínimo en las primeras horas de la mañana como se observa en la figura.
El "stress ácido" es uno de los principales efectos de un pH bajo, y se manifiesta por la excesiva acumulación de mucus en el tejido branquial que interfiere con el intercambio gaseoso y con una secuela que afecta al balance "ácido-base" de la sangre, causando "stress respiratorio" y disminución de la concentración de cloruro de sodio en la sangre, que a su vez causa disturbio osmótico.
A valores bajos del pH, la concentración del ión aluminio se incrementa en el agua y muchas veces los efectos tóxicos de este ión se adiciona a los efectos del pH.
Las branquias son también altamente sensibles al pH alto, manifestándose en una hipertrofia del epitelio de las branquias. A valores extremos del pH, 4 y 11, se produce la muerte, en tanto que el rango deseable para los cultivos está en 6,5 a 9.
La medición del pH se hace colorimétricamente, mediante una escala, o electrónicamente, mediante un potenciómetro (pH meter). El uso del papel de tornasol es una buena alternativa para determinaciones de campo. El mejor método para corregir niveles bajos del pH es el encalamiento del fondo del estanque o del agua misma.
