6.0 ABASTECIMIENTO DE ALEVINOS REPRODUCCION
Los peces nativos de la Cuenca Amazónica que se cultivan en América Latina, como la "gamitana", el "paco", el "boquichico", el "sábalo", entre otros, son reofílicos. Se desarrollan en los ambientes acuáticos laterales a los grandes ríos y cuando alcanzan su estado adulto y su madurez sexual, migran al río formando cardúmenes para desovar.
La reproducción se produce cuando las aguas comienzan a subir y el ambiente acuático se expande. Por lo tanto, estos peces viven y se desarrollan en un medio que experimenta cambios periódicos de luz, temperatura, salinidad, pH, oxígeno disuelto, lluvias, disponibilidad de alimentos, principalmente, que influyen de manera determinante en la maduración gonadal y en el éxito de la reproducción.
Para reproducirse, los peces necesariamente deben migrar a lo largo de los grandes ríos, por decenas de kilómetros, de otro modo sus gónadas se reabsorben. Por esta razón, no se reproducen espontáneamente en ambiente controlado, requiriendo de la administración de extractos hormonales, para inducir la ovulación y el desove.
En consecuencia, son dos las fuentes de abastecimiento de alevinos: el ambiente natural y la producción controlada con tratamiento hormonal.
En este capítulo se analiza en forma suscinta el abastecimiento de alevinos del medio natural, los mecanismos hormonales de la reproducción, el tratamiento de inducción, la incubación de huevos, obtención de larvas y los procesos de cría de larvas y alevinos, en ambiente controlado.
6.1 ABASTECIMIENTO DEL AMBIENTE NATURAL
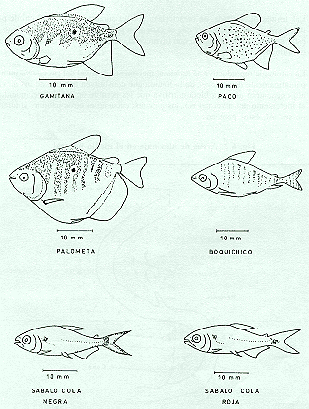
La piscicultura en la región se practicó en su inicio en base a alevinos capturados en el ambiente natural. Los principales peces que hoy se cultivan tienen su área de alevinaje en lugares accesibles donde pescadores especializados, principalmente en su identificación, concurren a colectar los alevinos deseados como los de "gamitana", "paco" "sábalo", "boquichico", "palometa", etc. (Fig. 6.1).
Sin embargo, el desarrollo de la piscicultura como actividad económica, en base a la oferta de alevinos del medio natural está limitado por el escaso número de ejemplares que pueden colectarse, más aún si tenemos en cuenta que de por sí dicha actividad es aleatoria, pero a la vez, es la única alternativa que tienen los piscicultores asentados en lugares alejados de los centros de distribución. Por otro lado, la conservación del acervo genético de las especies exige la combinación de poblaciones distantes; en consecuencia, la formación de reproductores en las estaciones de producción de alevinos debe sustentarse en alevinos obtenidos del ambiente natural o de lo contrario intercambiar reproductores entre las distintas estaciones, asegurándose que se traten de distintos linajes.
Fig. 6.1: Alevinos colectados en el medio natura
Las áreas de alevinaje de las especies nativas que se cultivan están constituidas por pequeños cuerpos de agua temporales y laterales al canal principal de los ríos de agua blanca (Fig. 6.2), por los remansos de la orilla convexa en charcos recientes influenciados por la resaca y que se encuentran en las playas, en los caños y quebradas que salen al cauce principal.
Las formaciones citadas se caracterizan por ser someras de 20 a 40 cm de profundidad con aguas tranquilas y que se extienden por la vegetación herbácea que puede estar en proceso de putrición, que favorece al crecimiento de organismos que sirven de alimento a los alevinos.
La estrategia reproductiva se asocia al incremento de nivel del río que va inundando paulatinamente depresiones de la llanura que constituyen hábitats de los alevinos y allí encuentran una rica biota nutritiva que les permite un rápido crecimiento. Con el incremento del nivel del río, los alevinos encuentran otros hábitats similares; de no ser así, éstos perecen.
Fig. 6.2: Areas de alevinaje en el medio natura

6.1.2 METODOS DE CAPTURA Y TRANSPORTE
La captura de los alevinos se realiza con una red pequeña denominada "alevinera", que se usa también para capturar peces ornamentales. Tiene una longitud de 2 a 5 m, 1,20 de alto y malla de 1/4" a menos; el hilo es de nylon muy fino, generalmente del número 3.
La red es operada por dos hombres que la arrastran hacia la orilla y al llegar a ella la levantan rápidamente, seleccionando los alevinos manualmente o con la ayuda de un cal-cal. Cuando abunda vegetación flotante y otros restos de vegetales se recoge con todo para luego eliminarlos.
El acopio y transporte de alevinos se realiza en cajas isotérmicas de tecnoport de 40 x 40 x 20 cm Puede usarse sin embargo otros equipos como tinas plásticas, cajas de madera forradas con plástico; vale decir, cualquier otro material que a juicio del pescador sirva para este fin.
Se recomienda recambiar el agua del recipiente con los alevinos a fin de eliminar agua con desechos y reponerlo con agua limpia y con buen contenido de oxígeno.
6.2 PRODUCCION CONTROLADA CON TRATAMIENTO HORMONAL
6.2.1 SOPORTE ENDOCRINOLOGICO DE LA REPRODUCCION
6.2.1.2 LA PINEAL Y EL HIPOTÀLAMO
La glándula pineal. También denominada epífisis, es una evaginación dorsal de la región diencefálica posterior del cerebro. Tiene función doble, sensorial y secretora. La función sensorial se realiza a través de células fotoreceptoras modificadas que reaccionan a la estimulación de las ondas electromagnéticas del espectro visible y no visible de la luz.
El hipotálamo. Está situado en la región ventral del diencéfalo. Sus células neurosecretoras responden a una señal eléctrica procedente del cerebro, liberando un mensajero químico en el extremo terminal del axón, llamado hormona liberadora. Este mensajero químico actúa sobre las células gonadotrópicas de la adenohipófisis. De esta manera el hipotálamo participa, en forma directa, en el control del proceso de reproducción, transformando la información nerviosa en hormonal.
La hipófisis o pituitaria, es una glándula clave en el control hormonal de la reproducción y de muchos otros procesos fisiológicos. Se encuentra situada en la zona ventral del diencéfalo, por detrás del quiasma óptico y por delante del saco vasculoso. Está íntimamente ligada al hipotálamo a través de conexiones neuronales y de vasos sanguíneos.
La glándula hipófisis está compuesta de dos partes: la adenohipófisis y la neurohipófisis.
Las hormonas de la hipófisis de los peces pueden ser divididas en dos grupos: uno que controla recíprocamente la función de otras glándulas endocrinas, y el otro que influye en procesos enzimáticos selectos en uno o varios tipos de células somáticas. En el primer grupo se encuentran, entre otras, las hormonas gonadotrópicas. En el segundo grupo hay varias hormonas que actúan sobre los melanóforos.
De este conjunto de hormonas, las que participan directamente en el proceso de reproducción son las gonadotrópicas que son producidas por la hipófisis como respuesta a la hormona liberadora del hipotálamo y son liberadas al torrente sanguíneo, para actuar a nivel de las gonadas estimulando la maduración de los gametos, acumulación de material de reserva y desencadenando el proceso de ovulación y desove.
Desde su origen y a través del tiempo, los peces, como muchos otros organismos, se han ido adaptando a la oferta ambiental, siendo más notorias las adaptaciones a las condiciones opuestas como el día y la noche, los días largos y los días cortos, la presencia o ausencia de las precipitaciones pluviales, la abundancia y escasez de alimento, entre otros.
La "gamitana", el "paco", el "boquichico" y muchos otros peces reofílicos en la Amazonía, han adaptado su período reproductivo hacia el comienzo de la expansión del ambiente acuático (ALCANTARA y GUERRA, 1 990), tal como ha sido reconocido en ecosistemas africanos por WELCOMME (1 980). En este período se presentan cambios ambientales importantes que implican intensificación de las precipitaciones pluviales, dilución y arrastre de nutrientes de los suelos adyacentes a los ambientes acuáticos, proliferación de microorganismos acuáticos, inundación de la floresta que conlleva alta descomposición de la materia orgánica, dispersión de los peces con lo que la predación disminuye, disminución de la temperatura media y del pH. Estímulos que en suma, son captados por los peces a través de los órganos de los sentidos, determinando la maduración de las gónadas, el comportamiento migratorio de los peces de los ambientes acuáticos cerrados hacia los grandes ríos y finalmente, la propagación de las especies. (Fig. 6.3).
Generalmente es par y en los teleósteos tiene forma de saco que se comunica con la papila genital a través del oviducto, como es el caso de los peces de condición cistovariana, como la "gamitana", el "paco", el "boquichico", entre otros. En el caso de los peces que no presentan oviducto, el ovario se comunica con la papila a través de la cavidad abdominal, en la que se vierten los óvulos, como es el caso de los peces de condición gimnovariana, ejemplo la "trucha".
Fig 6.3 ESQUEMA DEL MECANISMO NEURAL Y HUMORAL DE LA REPRODUCCION ESTIMULOS AMBIENTALES

Según el ritmo de desarrollo de los oocitos intra-ováricos, se han distinguido tres tipos de ovario:
a) Sincrónico total. En este tipo de ovario, todos los oocitos se encuentran en el mismo estadio de desarrollo, por lo que la maduración se produce en forma simultánea. El desove es total y ocurre sólo una vez en la vida del pez, como es el caso del "salmón" (Oncorhynchus).
b) Sincrónico en grupos. En este caso, el ovario contiene, por lo menos, dos grupos de oocitos en diferentes estados de desarrollo, observándose óvulos maduros de mayor diámetro y óvulos inmaduros de diámetro pequeño, constituyendo la reserva para un próximo período de desove. Como ejemplos se tiene la "gamitana" y el "paco".
c) Asincrónico. En este grupo se observan oocitos en el ovario en todos los estados de desarrollo. El desove, en este caso, es parcelado.
Como ejemplo se tienen varios cíclidos como "tilapia"; "tucunaré" (Cichla monoculus) y el "bujurqui" (Cichlassoma bimaculatum).
En el desarrollo de los oocitos en los Teleostos, en general, se distinguen dos fases: Fase pre-vitelogénica, que comprende dos estadíos:
La fase vitelogénica, en la que se forma y almacena el vitelo para reserva del futuro embrión y larva, tiene tres estadíos:
Cuando los oocitos están en proceso de maduración y en especial "en maduración final", son muy sensibles a cualquier tipo de "stress" a que esté sometido el pez y reaccionan interrumpiendo su desarrollo, seguido de un proceso de reabsorción del material celular a cargo de las células de la granulosa, que alcanzan un estado de hipertrofia. Como consecuencia de la atresia aparecen en la gónada femenina pigmentos amarillos grisáceos.
En la generalidad de peces los testículos son órganos pares, alargados. Tienen posición lateral o látero-superior en la cavidad abdominal a la cual están sujetos por tejido mesentérico.
El tamaño, el color y la sección transversal varían según sea el estado de madurez sexual, observándose el color blanquecino a blanco lechoso en los estadíos de maduración avanzada.
En la espermatogénesis las células germinales, poco diferenciadas o espermatogonias del testículo se transforman en células más elaboradas, así como los espermatozoides, que se caracterizan, en los teleósteos, por carecer de acrosoma. Esta característica está asociada a la presencia del micropilo en el óvulo, lugar por el que se realiza la penetración para la fecundación.
6.2.4 PREPARACION DE REPRODUCTORES
La preparación de reproductores se efectúa en estanques de tierra de superficie variable entre 600 y 2 500 m², con profundidades de 0,6 m a 1,2 m. El tipo de agua es también variable, entre agua negra, agua clara y agua blanca. En la Tabla 6.1, se presentan algunas variables de un estanque de agua negra utilizado en Iquitos, en la preparación de la "gamitana".
TABLA 6.1 VARIABLES FISICO QUÍMICAS DEL AGUA DE UN ESTANQUE DE REPRODUCTORES EN IQUITOS (Alcántara, 1991)
| VARIABLE | VALORES |
| Temperatura superficial (ºC) | 27,5 |
| Conductividad (umhos/cm) | 30,0 |
| Oxígeno disuelto (ppm) | 6,0 |
| Dióxido de carbono (ppm) | 3,0 |
| Nitrógeno amoniacal (ppm) | 0,7 |
| Dureza cálcica (ppm) | 19,9 |
| Dureza magnésica (ppm) | 0,1 |
| Alcalinidad total (ppm) | 10,0 |
| Hierro ferroso (ppm) | 0,2 |
| pH | 6,8 |
La "gamitana" y el "paco" toleran bajos tenores de oxígeno disuelto. Especialmente la primera soporta niveles tan bajos como 0,8 mg/l; en estos casos desarrolla una prolongación esponjosa del labio inferior, que le sirve para captar aire atmosférico directamente, mediante succión de agua y aire en la película superficial.
La densidad de carga más frecuente varía entre 200 a 300 g/m². Excepcionalmente se ha llegado a usar niveles de 1 000 g/m², como en algunas estaciones de Venezuela (Hernández, et. al. 1 992). Preferentemente, la preparación se efectúa en monocultivo, aunque en algunas estaciones de Brasil, Colombia y Venezuela se realiza también en policultivo.
La alimentación de la "gamitana" y el "paco" en esta etapa, se realiza con alimento artificial con un tenor de 30 a 35% de proteína total y 2 800 kcal/kg. En algunos casos la ración se basa en fórmulas específicas en base a insumos de disponibilidad local como harina de pescado, torta de soya, moyuelo de trigo, polvillo de arroz, harina de sangre de vacuno, maíz molido. Sin embargo, también se ha utilizado con buenos resultados, alimento preparado para gallinas ponedoras o alimento para trucha (ALCANTARA, 1 989).
La tasa de alimentación varía entre 3 a 5% del peso vivo; es decir, una "gamitana" de 6 kg. debe recibir de 180 a 300 g de alimento cada día.
El número de veces en que se ofrece alimento a los peces, varía según la disponibilidad de mano de obra o de facilidades en las estaciones de cultivo, tales como comederos automáticos. La práctica más corriente, en caso de ofrecer el alimento manualmente, es cuatro veces por día, aunque se han dado casos de oferta de diez veces por día (ALCANTARA, 1 985).
Dependiendo del grado de gordura de los reproductores, especialmente de la hembra, se ha reducido en forma ocasional la tasa de alimentación a 1% durante el último mes, previo al tratamiento hormonal para inducir la reproducción, como en el caso de oferta de alimento para trucha, ya señalado.
La forma de presentación del alimento es en "pelletz" con la suficiente aglutinación para mantener unidos los insumos alimenticios por unos segundos en el agua. La gamitana y el paco atrapan el alimento en el estrato superficial, por lo que es bueno buscar que el alimento tenga cierto grado de flotación lo que se consigue con una buena aglutinación en el momento del peletizado o con la adición de aceite y aglutinantes.
El tamaño de la partícula es también importante en la alimentación de los peces. Frecuentemente se utilizan "pelletz" con un diámetro de 5mm, con buenos resultados, aunque se han observado casos en que se han utilizado peletz de 10 mm. Sin embargo, no debe usarse partículas demasiado grandes, aún cuando sea en grumos, ni mucho menos alimento en polvo, ya que el aprovechamiento como es obvio no será adecuado, ocasionando como resultado, pérdida de una buena parte del alimento.
Siendo necesario efectuar el reajuste periódico de la cantidad de alimento a suministrar a los peces, es una práctica corriente la ejecución de muestreos. En este caso, cuando se aproxima el período de reproducción, el muestreo se realiza con mucho cuidado, evitando capturar toda la población y en especial, los traumatismos y el manipuleo excesivo o cualquier causa que pueda devenir en "stress" de los peces y en interrupción del proceso de maduración de los oocitos.
La "gamitana" y el "paco" en el área de Iquitos, alcanzan su madurez sexual a la edad de 4 años y el "boquichico" lo hace en el primer año. Sin embargo, se han reportado casos de madurez de machos de gamitana y paco en 2-4 años y de hembras en 3-4 años (HERNANDEZ et. al. 1 992).
Asimismo la duración del período de maduración es variable. En Iquitos se tiene una duración de cinco meses que corresponde al período comprendido entre octubre y febrero, época en que se registra incremento de las precipitaciones pluviales. En este sentido, según las condiciones climáticas locales de las áreas de cultivo de la gamitana y el paco, se han reportado variaciones, registrándose casos en que cubre todo el año, como en la estación de Betume-Brasil (HERNANDEZ et. al. 1 992).
6.2.5 LA REPRODUCCION INDUCIDA
6.2.5.1 SELECCION DE LOS REPRODUCTORES
En la selección de la hembra de "gamitana", "paco" o "boquichico", para el tratamiento hormonal, con fines de inducción de ovulación y desove, se aplican con frecuencia dos criterios: a) observación de la posición del núcleo del oocito y b) observación de los caracteres externos de madurez sexual.
En el primer caso, a través de las diferentes fases de desarrollo gonadal, los oocitos muestran su núcleo en posición central o periférica (Agostinho et. al. 1 982). Un oocito con su núcleo en posición central es inmaduro y en posición periférica, maduro. En este sentido se practican biopsias del ovario por vía intraperitoneal o genital, para extraer pequeñas muestras de oocitos. Estas muestras se lavan en solución fisiológica (cloruro de sodio al 0,6%) y luego se colocan en solución serra (60% de alcohol, 30% de formol y 10% de ácido acético glacial), para su observación en una lupa estereoscópica; la solución serra permite la aclaración de la membrana y el citoplasma del oocito, haciendo posible la visualización de la posición del núcleo y consecuentemente la definición de la inmadurez o madurez del oocito.
Los peces cuyos oocitos tienen el núcleo en posición periférica responderán positivamente al tratamiento hormonal.
En el segundo caso, la observación de los caracteres externos de madurez sexual, aunque es un criterio subjetivo, ha sido muy utilizado desde que FONTENELE (1 959) estableció los criterios para Prochilodus cearensis y aún se sigue aplicando.
En la selección se tiene en cuenta el grado de desarrollo del vientre así como el grado de tensión. En tal sentido se seleccionan hembras con vientre dilatado y suave al tacto, cuando se ejerce una ligera presión. En algunos casos se ha considerado la dilatación y el enrojecimiento de la papila genital, pero estos caracteres no son seguros ya que pueden deberse a un intestino cargado y próximo a ser evacuado, así como al rozamiento de la papila en la red utilizada para la captura.
Como se puede apreciar, el éxito en la selección según este método, está supeditado a la habilidad y experiencia del operador.
Los machos de "gamitana", "paco" o "boquichico" presentan evidencias de maduración antes que las hembras, emitiendo esperma blanquecino lechoso cuando se ejerce una ligera presión del abdomen en las proximidades de la región uro-genital. En esta operación se debe tener cuidado de no deslizar la mano, si no tan solo ejercer presión; de otro modo se producirá desprendimiento de escamas en la zona tocada.
Los machos que presentan esperma blanco lechoso denso deben seleccionarse para ser sometidos a tratamiento hormonal, descartándose los que presenten un color viscoso y fluidez del esperma.
Se han utilizado como inductores de la reproducción tanto extractos hipofisiarios de la misma especie como de otras. Asimismo, se han utilizado gonadotropina coriónica humana (GCH) y "hormona liberadora de hormonas gonadotrópicas (LHRH o GnRH) y sus homólogos y análogos" (HERNANDEZ, et. al. 1 992).
La "gamitana" y el "paco", por tanto, son peces receptores de amplio espectro cuya especificidad hormonal no parece tener mucha importancia.
La inoculación de extractos de glándula hipófisis es una práctica generalizada, con muy pocas variaciones en cuanto a la dosificación, preparación del extracto, número de inyecciones, intervalo y vías de administración.
La colección de hipófisis debe efectuarse de donadores sexualmente maduros a fin de obtener glándulas con altas concentraciones hormonales. La glándula se ubica en el piso de la cavidad craneana, en la "silla turca", por detrás del quiasma óptico y delante del saco vascular del diencéfalo. Levantando la masa encefálica, resulta relativamente fácil la localización de la hipófisis, mediante los puntos de referencia señalados, pero fundamentalmente con la pericia y experiencia del operador.
La preservación de la glándula se efectúa ya sea en acetona o en alcohol absoluto. En el primer caso, luego de la extracción se lava las glándulas por tres veces con la finalidad de eliminar la mayor cantidad de grasa y una vez limpias y deshidratadas se pueden guardar secas, a temperatura ambiental. En el segundo caso, las glándulas se lavan en alcohol absoluto por tres veces como mínimo y luego se guardan en alcohol, en un frasco oscuro.
La dosis general para inducir la ovulación y desove es de 5 a 6 mg/kg., aunque en el Nordeste de Brasil se ha llegado a usar hasta 7 mg/kg. (HERNANDEZ, et. al. 1 992). La dosis mínima se utiliza para individuos de 4 a 8 kg. y las dosis de 6 a 7 mg/kg. se utiliza en hembras de 8 a 10 kg. Es poco recomendable utilizar individuos mayores de 10 kg., tanto por la dificultad de manipulación, como por la gran demanda de extractos hormonales. Los machos requieren una dosis menor y responden bien al tratamiento con l mg/kg.
La dosis total en las hembras se administra en dosis parciales. Una estimulante equivalente al 10% y una desencadenante correspondiente al 90%. En los machos la dosis total es administrada en dosis parciales de 50% cada una. El intervalo de aplicación de ambas dosis varía entre dieciocho a veinte horas.
En cada dosis se utiliza como vehículo de 0,5 a 1,0 ml de agua destilada estéril o suero fisiológico.
Las vías de inoculación más utilizadas son la intramuscular y la intraperitoneal. La intramuscular se aplica en los músculos dorsales delante y detrás de la aleta dorsal y la intraperitoneal se administra en el pliegue de origen de las aletas pectorales o ventrales. Sin embargo la intramuscular está quedando en desuso porque cuando se usa como vehículo más de 0,5 ml, parte del extracto se pierde por la presión y resistencia intramuscular.
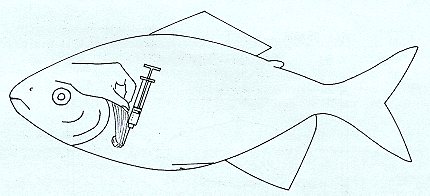
En la inyección intraperitoneal, de otro lado, se debe tener cuidado de no lesionar órganos vitales. (Fig. 6.4).
Fig. 6.4: Administración del extracto hormonal por vía intraperitonea
Otro inductor que se está usando en forma creciente es la hormona sintética de uso veterinario acetato de buserelina, conocida comercialmente como Conceptal. Esta hormona actúa a nivel de la hipófisis estimulando la liberación de las hormonas folículo estimulante (FSH) y luteinizante (LH).
La dosis total para la hembra, tanto en "gamitana" como en "paco" y "boquichico" es de 2,6 ml/kg., dividida en dos dosis parciales de 10% y 90% y la dosis para el macho es de 1,0 ml/kg., dividida en dos dosis de 50% cada una.
El intervalo de administración de las dosis parciales es de doce horas tanto en la hembra como en el macho. La vía de inoculación en este caso, debe ser siempre la peritoneal, por tratarse de un gran volumen. Con este tratamiento, la ovulación y el desove se producen en términos generales, en el mismo período que en el tratamiento con extractos de hipófisis.
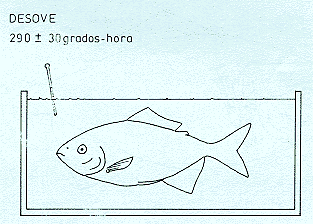
La ovulación y desove se realiza a las 11 ± 2 horas ó 290 a 320 hora grados. WOYNAROVICH (1 981), recomienda la práctica de sutura de la papila urogenital para lograr mayor eficiencia en la colección de óvulos; sin embargo, esta práctica no es generalizada y algunos operadores prefieren prescindir de ella, manteniendo vigilada a la hembra en los instantes próximos al desove. (Fig. 6.5).
Fig. 6.5: Control de grados-hora para el desov
Al cumplirse las hora-grados para el desove, se retira la sutura o se captura con cuidado a la hembra, cubriendo de inmediato con una mano la abertura urogenital para evitar la pérdida de óvulos. En esta operación, se seca a la hembra con una toalla suave para eliminar el agua, se presiona ligeramente los costados del cuerpo para la obtención de los óvulos que se reciben en una bandeja pequeña. En ese instante debe tenerse cuidado de no deslizar las manos para no ocasionar la pérdida de escamas (Fig. 6.6).
Fig. 6.6: Procedimiento para ayudar el desove de los pece

Eventualmente, en hembras tratadas durante 4 a 5 campañas, se han observado estructuras residuales de las gónadas, de aproximadamente, 5 cm de longitud, de consistencia dura, en forma de V y de sección triangular en cada una de sus ramificaciones. Estas estructuras se localizan en la parte inferior del vientre con el vértice dirigido hacia la abertura genital, constituyendo un verdadero tapón. En estos casos, al llegar el momento del desove, primero emerge el "tapón" y al retirarlo con la mano, el desove se realiza normalmente.
En casos de sobredosis, son frecuentes los cuadros hemorrágicos a nivel del tegumento de la región abdominal y los prolapsos que determinan la muerte de la hembra y en casos de dosis inferiores a la óptima, puede presentarse ovulación parcial y desove prolongado que implican pérdida de óvulos. En estos casos es necesario mantener a la hembra en observación por un período adicional de 24 horas para proceder a "limpiarla" con presión ligera del vientre, para eliminar los óvulos libres sobremadurados y retenidos, que de otro modo ocasionarán procesos infecciosos y pérdida del pez.
Finalizado el desove, se extrae al macho y se le seca también con una toalla suave, para luego obtener esperma ejerciendo ligera presión del vientre, a la altura de los testículos. Con el tratamiento descrito anteriormente, se obtiene una buena espermiación de los machos; por eso se trabaja con un macho para una hembra.
Una vez que se logra el esperma, se vierte directamente sobre los óvulos, iniciándose la fecundación y formación del huevo. El esperma y los óvulos se mezclan en seco, por espacio de 1 a 2 minutos con una pluma de ave (Fig. 6.7). En este tiempo, los espermatozoides pierden su motilidad y la superan cuando se añade una pequeña cantidad de agua, continuándose la mezcla por espacio de 1 a 2 minutos más.
Fig. 6.7: Fecundación: mezcla de los productos femenino y masculino con la ayuda de una pluma de gallina

Cuando los huevos entran en contacto con el agua, se acelera el proceso de hidratación o incorporación de agua, con lo cual el diámetro se incrementa de 1,0 mm a 4 mm, en promedio. En este proceso, se produce el cierre del micropilo y a partir de este momento ya no es posible la fecundación. Los óvulos se hidratan al contacto con el agua, y no es posible diferenciarlos en las primeras horas después de la fecundación, ya que también puede presentarse falsa segmentación. Sin embargo, al cabo de 3 o 4 horas empiezan a degenerarse y morir los óvulos no fecundados, adoptando una apariencia blanca algodonosa diferente de los huevos fecundados y vivos que presentan un aspecto refringente y translúcido.
A fin de tener la certeza de la calidad del esperma, es una buena práctica examinar una gota a través del microscopio, para visualizar la motilidad de los espermatozoides, sobre todo, si se trata de un esperma obtenido antes del desove, sin y con adición de agua. La falta de movimiento de los espermatozoides indica su inactivación.
1. El agua
El agua para la incubación de los huevos, en lo posible debe ser carente de sólidos en suspensión y de materia orgánica, sea viva o inerte, ya que de otro modo, estos materiales se depositan sobre la superficie de los huevos, limitando el proceso de respiración que se realiza a través de la membrana.
El uso de agua de pozo o de manantial es una buena alternativa. En la estación del Instituto de Investigaciones de la Amazonía Peruana-IIAP, en Iquitos, se utiliza agua de manantial, cuyas características se señalan en la Tabla 6.2.
TABLA 6.2 PARAMETROS FISICO-QUIMICOS DEL AGUA UTILIZADA EN INCUBACION DE HUEVOS DE "gamitana" y "paco", EN IQUITOS (ALCANTARA, 1991)
|
PARAMETRO |
NIVEL |
|
Temperatura superficial ( C) |
25,00 |
|
Conductividad (umhos/cm) |
40,00 |
|
Oxígeno libre (ppm) |
4,00 |
|
Dióxido de carbono libre (ppm) |
11,00 |
|
Nitrógeno amoniacal (ppm) |
0,35 |
|
Dureza cálcica (ppm) |
19,00 |
|
Dureza magnésica (ppm) |
1,00 |
|
Alcalinidad total (ppm) |
20,00 |
|
Hierro ferroso (ppm) |
0,175 |
|
p |
5,6 |
|
Colo |
Té oscur |
Debe tenerse cuidado con el nivel de pH en el agua de pozo, ya que con niveles menores a 5,5 se presentan altos contenidos de CO2 que se adhiere a los huevos en forma de burbujas y cada burbuja constituye un punto de ligazón con otros huevos, que llegan a formar paquetes, emergiendo hasta la superficie. En estos casos se debe recurrir al encalamiento del agua, para alcanzar un pH cercano al neutro, con lo que baja el CO2, formándose los bicarbonatos y carbonatos, desapareciendo el problema.
2. Incubadoras
Las incubadoras son recipientes cónicos o cilindro cónicos, de materiales diversos como: vidrio, fibra de vidrio, plástico y en general, de cualquier material inerte.
WOYNAROVICH (1 981), describe una incubadora que es muy utilizada, pero se puede usar otra más sencilla (Fig. 6.8). En cualquier caso, una incubadora debe funcionar con abastecimiento constante de agua, a fin de mantener los huevos en movimiento ya que de otro modo se adhieren entre si y mueren; adicionalmente, la renovación constante del agua permite eliminar los catabolitos, como dióxido de carbono y amoníaco.
Fig. 6.8: Incubadora de huevos de peces reofílicos

El ingreso de agua a las incubadoras es por la base cónica y la salida es por rebose, captándose en un canal colector. (Fig. 6.9).
Fig. 6.9: Batería de incubación: (1) Incubadoras; (2) Canal de colecta; (3) Colector de larvas; (4) Sifón; (5) Balde
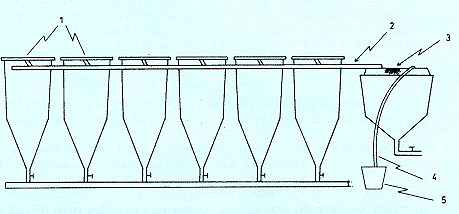
Dependiendo de la disponibilidad de agua, se han utilizado incubadoras de diverso tamaño, desde 6 hasta 200 litros.
3. Flujo de incubación
El flujo de incubación debe ser lo suficiente como para provocar el movimiento lento de los huevos en la zona cónica de la incubadora, únicamente. No se debe usar el flujo muy alto y capaz de producir un movimiento intenso de los huevos, más allá de la zona cónica, porque resultará perjudicial. En todo momento, debe tenerse presente que los huevos son muy delicados y que los traumatismos producidos por el flujo excesivo interrumpen el desarrollo embrionario y producen mortalidad. El flujo excesivo durante el estadío de mórula por ejemplo, produce desprendimiento de algunas células y luego el huevo muere.
En la estación del IIAP, en Iquitos, se aplica un flujo de 0,6 1ñ 0,1 litro por minuto, en incubadoras de 60 litros.
4. Carga por incubadora
En cada incubadora se colocan de 30 a 50 gramos de huevos recién fecundados sin adición de agua; esto significa de 30 000 a 50 000 huevos. Una vez efectuada la carga de las incubadoras no se debe realizar trasvase de huevos, de otro modo, se producirá la rotura del corion y por lo tanto, la muerte de muchos huevos.
5. Desarrollo de los huevos
Producida la fecundación, en unos pocos minutos se produce la hidratación final de los huevos al contacto con el agua; al mismo tiempo, se produce la polarización, distinguiéndose nítidamente el polo animal o germinativo del polo vegetativo.
La división celular se produce en el polo animal observándose el primer clivaje a los 15 minutos, que da lugar al estadío 2 células. La división celular y el desarrollo embrionario son continuos y si las condiciones de abastecimiento de agua, con buen tenor de oxígeno se mantienen con una temperatura media de 26 C, el desarrollo se completa, produciéndose la eclosión y salida de la larva en 18 horas.
El desarrollo embrionario (Fig. 6.10) es un proceso de temperatura dependiente. Se acelera cuando se incrementa la temperatura y es más lento cuando ésta disminuye; sin embargo, las temperaturas extremas superiores a 30 C, pueden ser letales.
6. Comportamiento larval y separación
En el momento de la eclosión, las larvas salen con características peculiares, tales como: la boca y los opérculos que están parcialmente desarrollados, no tienen pigmentación y el intestino no ha completado su desarrollo. Ascienden poco a poco, con movimientos propios y ayudadas por la corriente de agua para luego descender por la gravedad; de cuando en cuando reposan por varios segundos en el fondo.
Fig. 6.10: Desarrollo embriológico y larva
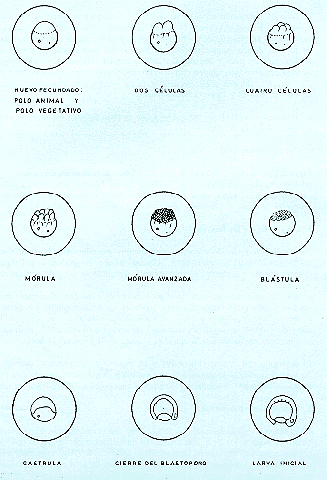
Con este comportamiento, cuando alcanzan la capa superficial de agua, salen arrastradas por la corriente al canal colector y a través de él llegan al colector de larvas. Durante las 8 a 10 horas siguientes a la eclosión las larvas pasan al colector con agua limpia y en las incubadoras quedan unas pocas larvas, conjuntamente con los huevos muertos y corion ("cascaras" de los huevos).
Las larvas son sembradas luego de la separación, en jaulas pequeñas de 3,0 x 1,0 x 0,2 m, con malla de 300 micras, colocadas en la zona litoral del estanque. En las jaulas permanecen durante tres días, en que no ingieren partículas alimenticias, consumiendo sólo sus reservas nutritivas del saco vitelínico.
Las jaulas se fijan a estacas y están protegidas de la incidencia directa de la luz solar, mediante hojas de palmeras como Mauritia flexuosa.
Al cuarto día las larvas presentan pigmentación en el tegumento, el opérculo está más desarrollado, el intestino se abre y la vejiga gaseosa se llena de aire, presentando la apariencia de una burbuja.
En este momento las larvas empiezan a nadar en sentido horizontal y a la vez, inician la captura de su alimento natural compuesto por plancton, por lo que son liberadas en el estanque de larvicultura previamente tratado.
Al momento de la siembra en las jaulas se efectúa una estimación del número, de acuerdo a ROTHBARD (1982):

donde:
K=número de muestras (K 1)
ni=número de larvas en la muestra
V=volumen del recipiente de larvas
N=número total de larvas
En las jaulas se colocan 10 000 larvas/m² y al liberarlas en el estanque la densidad baja a 200-400 larvas/m².
1. Preparación de estanques
Los estanques de larvicultura deben prepararse con anterioridad a la siembra, preferentemente de 8 a 10 días antes, a fin de producir en este tiempo, las más altas densidades de micro organismos componentes del plancton, de mayor interés, como los Rotíferos del género Brachionus. Después de este período empiezan a incrementarse considerablemente los componentes secundarios del plancton como los Cladóceros y los Copépodos, entre otros organismos, declinando los rotíferos.
La preparación de los estanques implica el vaciado total, la fertilización y llenado. La eliminación de peces se puede conseguir con aplicación de rotenona a una concentración de 0,1 a 0,25 ppm (2 a 5 ppm de rotenona al 5%). Esta sustancia pierde su poder letal en 2 ó 3 días, después del cual puede llenarse nuevamente el estanque. Otra forma de eliminar los peces de los estanques de larvicultura es mediante la aplicación de 1 000 kg./ha de cal apagada o cal viva, estando el suelo húmedo y en especial, en los charcos que no pueden vaciarse por completo. En estos casos, la cal forma hidróxidos de calcio que elevan la alcalinidad hasta alcanzar un nivel letal. Con este tratamiento es necesario dejar el estanque vacío por lo menos una semana antes de llenarlo nuevamente. Complementariamente, la cal ayuda a corregir el pH en suelos ácidos, mejorando la productividad.
Se puede aplicar también fertilizantes inorgánicos como orgánicos para mejorar la productividad. Los fertilizantes orgánicos están disponibles en cualquier área. Por ejemplo se pueden aplicar 1 000 a 1 500 kg./ha de gallinaza y 500 a 1 000 kg./ha de hierbas, tales como gramíneas y otros que crecen en el entorno del estanque. Con el tratamiento antes descrito, en Iquitos, se alcanza niveles de producción de planctontes del orden de 32 000 organismos por litro, compuesto preferentemente por Moina p. (Cladócera), que permite una buena sobrevivencia en la fase larva- levino. (Fig. 6.11).
2. Siembra de larvas
La siembra de los estanques de larvicultura se realiza con larvas de 3 días a razón de 200 a 400 larvas por metro cuadrado. Desde la siembra hasta el décimo día, las larvas sólo se alimentan de microorganismos disponibles en el estanque.
Al cabo de este período, las reservas del saco vitelínico están virtualmente agotadas y la larva ha crecido y se ha transformado en un pececillo o alevino de más o menos 1 centímetro de longitud.
3. Alimentación de larvas
A partir del décimo día se proporciona alimento artificial en polvo, con un tenor de proteína de 30% compuesto por los mismos insumos antes citados, con excepción de maíz, moyuelo y harina de sangre. También se ha utilizado alimento preparado para gallinas ponedoras finamente molido y tamizado. La cantidad de alimento que se ofrece cada día debe ser estimada, pudiendo empezarse con 4 g por metro cuadrado durante las dos primeras semanas para incrementar la cantidad al doble durante los quince días siguientes. Otra forma de alimentar los alevinos es proporcionando alimento "ad libitum", esto es, suministrando alimento hasta que los alevinos muestren indiferencia.
Fig. 6.11: Alimento inicial de larvas de gamitana y pac

4. Eliminación de predadores
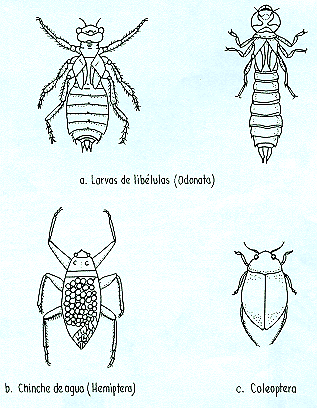
Con frecuencia, en estanques que tienen agua por más de quince días, aparecen conjuntamente con los organismos planctónicos o infiltrados desde estanques contiguos, una serie de insectos en fase larval o adulta, que devienen en predadores, por lo que su control es una necesidad crítica, a fin de lograr la mayor sobrevivencia de alevinos.
En general, estos insectos se agrupan en dos categorías: a) de respiración traqueal y b) de respiración branquial. Los de respiración traqueal requieren de aire atmosférico que lo captan ascendiendo a la película superficial y los de respiración branquial requieren de oxígeno disuelto en agua. En el primer grupo están una serie de insectos adultos de los órdenes Hemíptera (Belostoma sp., Nepa sp., Notonecta sp.), Díptera (Culex sp., Anopheles sp., Chironomus sp.) y Coleóptera (Dityscus). En el segundo grupo, están las fases larvales de insectos del orden Odonata, tales como Gomphaeshna anax, Libellula sp., Sympetra sp., Sphylla sp., Tramea calverti, T. cophysa, Miathyra marcella y otras (Delgado, et. al. 1994 ). (Fig. 6.12).
Para erradicar los insectos de respiración traqueal se aplican dosis de 10 a 15 litros por hectárea de kerosene, diesel o un lubricante ligero; incluso se puede usar aceite quemado de motor.
Estas sustancias forman una película aceitosa sobre la superficie del estanque, dificultando la captación de aire para el proceso respiratorio, muriendo los insectos por asfixia.
La erradicación de los insectos de respiración branquial requiere de la aplicación de insecticidas en el agua. Entre éstos tenemos varios de tipo orgánico fosforados, tales como Dipterex, Dylox, Masotén, Flibol, que se aplican en dosis de 0,25 a 1,0 mg/l (WOYNAROVICH, 1 981).
ANOTACION
| 1. SOLUCION FISIOLOGICA: | Solución de cloruro de sodio al 0,6% |
| 2. SOLUCION SERRA: | 60% alcohol |
| 30% formol | |
| 10% ácido acético glacial |
Fig. 6.12: Predadores de larvas y alevinos de gamitana y paco